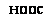Для питания, т. е. для основного обмена грибов, необходимо приблизительно 17—18 элементов, в число которых входят азот, углерод, кислород, водород, сера, фосфор, калий, магний, железо, медь, цинк, марганец, молибден, кальций. Вероятно, им также нужно немного кобальта, а по некоторым данным, и галлий, бор, скандий, ванадий. В специальных синтезах (экологического значения) участвует также хлор, например в синтезе хлорсодержащих антибиотиков гризеофульвина и геодина. Возможно, что роль его и более широка.
В большом количестве грибам требуются следующие основные элементы: азот, углерод, кислород, водород, фосфор, калий, сера и магний. Поэтому в питательные среды на водопроводной воде, где достаточно микроэлементов, добавляют кроме источников азота и углерода только фосфорнокислый калий и сернокислый магний (источники калия, фосфора, серы и магния).
Методы изучения потребностей грибов в минеральных компонентах специально разработаны рядом авторов (Lilly, 1965),
Классический метод (разработан Суейнбергом) состоит в испытании на синтетической среде, очищенной от следов минеральных компонентов, с точной их дозировкой. Учет потребности в них производится в основном по интенсивности роста организма.
Функциональный метод состоит в определении элементов, необходимых для функции определенных энзимов. Исследуется способность этих элементов образовывать комплексы с энзиматическими белками, например, прн использовании метода парамагнитной электронно-резонансной спектроскопии (Nicholas et al., 1962) изучалось образование белковых комплексов у бактерий с железом, марганцем, молибденом и медью.
В работах с минеральными компонентами необходимо учитывать два момента.
1. Возможность биологического замещения одного компонента другим. Полное замещение встречается редко, но частичное наблюдалось. Таким образом, можно не выявить потребность в элементе, если в среде есть его заместитель. Например, в питании Allomyces arbuscula (штамм Burman IDb) кальций можно полностью заменить хромом, стронцием, но стронция требуется в 10 раз больше, чем кальция (Lilly, 1965).
Аналогичное явление отмечено для замены цинка при синтезе протеинов, триптофана и других ароматических аминокислот через кадмий у Aspergillus niger (Bertrand, De Wolf, 1960). Калий частично замещается у A. niger натрием.
2. Возможность антагонизма ионов. Концентрация необходимого иона может зависеть от концентрации другого иона. Например, для Saccharomyces carlsbergiensis при увеличении концентрации натрия в среде нужно увеличивать и концентрацию калия для получения оптимальных условий роста. В результате увеличения концентрации натрия уменьшается усвояемость
калия.
Накопление кобальта и никеля в клетках Torula (Candida) зависит от концентрации в среде магния (Lilly, 1965).
По требуемым количествам элементы питания делят на макроэлементы и микроэлементы. После азота, углерода, водорода, кислорода наиболее важные макроэлементы — фосфор и сера. Они участвуют почти во всех биохимических реакциях в живых организмах как энергодающие системы или акцепторы в процессах биосинтеза (при конденсации, циклизации, окислении, восстановлении и т. д., являясь компонентами коферментов).
|
Н2С—SH |
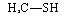 Сера играет большую роль в структуре клеток, так как она входит в состав белков в виде серосодержащих аминокислот: цис — тина, метионина и др. Сера обеспечивает конформацию, т. е. пространственную конфигурацию ферментных белков, связывая части полипептидной цепи —S—S-мостиками. Она входит в состав очень реактивных сульфгидрильных соединений (содержащих свободную SH-группу), являющихся источниками водорода при восстановительных реакциях. Тип их трансформации можно видеть на примере превращения цистеина в цистин:
Сера играет большую роль в структуре клеток, так как она входит в состав белков в виде серосодержащих аминокислот: цис — тина, метионина и др. Сера обеспечивает конформацию, т. е. пространственную конфигурацию ферментных белков, связывая части полипептидной цепи —S—S-мостиками. Она входит в состав очень реактивных сульфгидрильных соединений (содержащих свободную SH-группу), являющихся источниками водорода при восстановительных реакциях. Тип их трансформации можно видеть на примере превращения цистеина в цистин:
НаС—S——————- S сн2
-Н,
|
2 НС—NHa |
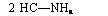 — не—nh2 h2n—CH
— не—nh2 h2n—CH
|
|
|
ноос |
Цистин
Так же функционирует трипептид-глютатион, составленный из
-Н,
глютаминовой кислоты, глицина и цистеина: 2GSH—— ► GS—SG
Строение глютатиона:
НООС—CH—СН2—СО— NH—СН—СО—NH—СН2
|
nh2 |
|
Глицин |
![]()
|
Цистенн |
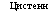 Глютаминовая кислота
Глютаминовая кислота
Другая функция серы состоит в стимуляции протеолитических ферментов, а отсюда и участие сульфгидрильных соединений в делении клеток. Поэтому БН-соединений много в молодых клетках. По некоторым данным, старение белков зависит от понижения их реактивности вследствие образования обильных мостиков ди-
|
35 |
![]() 2*
2*
Извлекаемые из грибов ферменты, содержащие 8Н-группы (Диксои, Уэбб, 1982)
|
Класс ферментов |
Фермент |
Кофак торы |
Реакция |
Источники |
|
цитохромоксидаза (цитохром а3) |
глюта- тион Си |
4-ферроцитохром с + 02 = = 4-феррицитохром с+2НгО |
широко распростра нены |
|
|
Окси- дазы |
цитохромперокси- даза |
глюта- ТИОН Ре2+ |
2-ферроцитохром с + Н2Оа = = 2-феррицитохром с+2Н20 |
плесневые грибы и дрожжи |
|
каталаза |
глюта- тиои рег+ |
2Н202 = 02 + 2НгО (донором Н2 может быть этиловый спирт) |
широко распростра нены |
|
|
Транс- феразы |
гликоген-УДФ-глю- козилтрансфера за |
БН Мё2+ |
УДФ-глюкоза-(-(гликоген)га= =УДФ+(гликоген)„+1 |
дрожжи |
|
метионинаденозил- трансфераза |
ЭН Л^2+М+ |
АТФ + Ь-метионии + Н20 = =ортофос*ат+пирофосфат + 4 Б — аденЬзилметионин |
дрожжи |
|
|
Лиазы |
изоцитратлиаза |
БН Л^2+ |
Ь — изоцитрат=сукцинат+гли — оксилат |
плесневые грибы и дрожжи |
|
Г идрата — зы и дегидра- тазы |
аконитатгидратаза (аконнтаза) |
БН Ре2+ |
цитрат= цнсакоиитат+ Н20 |
широко распростра нены |
|
дегидратаза диокси- кислот |
БН М2+ |
2.3-диоксиизовчлерианат =2- оксоизовалерианат+ Н20 |
плесневые грибы и дрожжи |
|
|
имидазолглицеро- фосфатдегидратаза |
БН Мп2+ |
О-эритроимидазолглицеро- фосфат=имида золацеталь — фосфат Н20 |
плесневые грибы |
|
|
Изоме- разы |
изопентенилпиро — фосфат изомераза |
БН Мб2+ |
диметилаллилпирофосфат= и зопентенилпирофосфат |
дрожжи |
Примечание. М2+ и М+—двух — и одновалентные металлы.
сульфида —S—S—, тогда как активная форма содержит SH-rpyn — пы. Сера входит в состав ряда витаминов: тиамина, биотина и ко — энзима А, участвующего в обмене кислот цикла Кребса, жирных кислот, липоидов и терпенов. Почти все реакции конденсации с присоединением двууглеродных фрагментов идут с участием КоА.
SH-группы являются необходимыми коферментами очень большого количества энзимов, чаще оксидаз, дегидрогеназ и гидратаз, присоединяющих воду (табл. 2.1). Часто функция SH-группы состоит в удерживании субстрата реакции в контакте с производящим реакцию коферментом (например, витамином) или в фиксации кофермента на апоферменте.
Сера в грибах (и в других организмах) в подавляющем числе случаев находится в восстановленной форме как производное сероводорода H—S—Н, но источником ее могут служить только окисленные соединения (ионы S042- и SCV-), далее восстанавливаемые грибами. Сульфиды металлов (FeS, Na2S), как правило, непригодны для питания грибов. Исключение составляет Cerato — stomelia multiannulata (Ophiostoma multiannulatum), не усваивающая сульфатов, а только сульфид аммония, цистин и цистеин (Лилли, Барнетт, 1953) и сапролегнии, нуждающиеся в серосодержащих аминокислотах. По Волконскому (Фостер, 1950), они относятся к паратиотрофам, а усваивающие сульфаты — к эутиотро — фам. Сера требуется при добавлении ее в питательные среды в сотых или тысячных долях процента, но количество ее в клетках меняется в зависимости от ее концентрации в среде и от концентрации азота (так как она входит в состав белков) и может колебаться от 0,1 до 0,5% от массы сухого мицелия (Lilly, 1965).
Фосфор входит в виде ортофосфорной кислоты в нуклеопротея — ды, функцией которых является передача наследственных свойств и синтез белков. В связи с этим он необходим всем живым организмам. В табл. 2.2 представлены обнаруживаемые у грибов содержащие фосфор нуклеопротеиды.
Накопление нуклеотидов в мицелии грибов соответствует преобладающему у данного вида или в данной фазе развития обмену. Например, у хитинообразующих грибов обилен уридинфосфатаце- тилглюкозамин (УДФАГ) в богатых жиром склероциях спорыньи (Claviceps purpurea) — цитидинфосфат, у дрожжей и в молодом мицелии Pйnicillium chrysogenum — АТФ (Белозерский, Кулаев, 1964; Крицкий, 1965; Мансурова, 1966). Датчиками энергии фосфорных связей обычно являются трифосфаты нуклеотидов (реже дифосфаты), но у грибов как источники энергии (связи —О—Р—) еще широко используются неорганические полифосфаты, описанные в первой главе, накапливающиеся в мицелии иногда в очень большом количестве (Кулаев, 1975).
Фосфат является также обязательной составной частью большинства кофакторов окислительных, восстановительных, гидролитических и декарбоксилирующих коферментов, например НАД и НАДФ. Хотя роль фосфора как непосредственного кофактора ферментов кажется незначительной (табл. 2.3), однако почти ни одна
|
Нуклеотиды, обнаруживаемые в кислоторастворимон (в холодной хлорной или трихлоруксусиой кислотах) фракции Реп1с1Шит сЬ. гу$о£епит или Д^аг/смв Ыврогив
|
|
Примечание. Обозначения в списке сокращений. ГМФ — нофосфат. гуанозинмонофосфат. |
|
Т а б л и ц а 2.3 Извлекаемые из грибов ферменты, активируемые фосфором (по Диксону и Уэббу, 1982)
|
ферментная реакция не обходится без фосфора как донора энергии. Весь обмен углеводов идет при обязательном фосфорилиро — вании всех видов сахаров от триоз до седогептулозы, с присоединением от одной до двух молекул фосфорной кислоты, например, глюкозо-6-фосфат, фруктозо-1,6-дифосфат и т. д. С участием фос — форилирования протекают все процессы брожения и дыхания.
Вместе с азотсодержащим спиртом и жирными кислотами фосфор входит в состав фосфолипидов и других эфиров, например фитина (фосфорного эфира инозита).
Фосфор усваивается грибами в виде Р042-, органических фосфатов и фосфатэфиров и требуется при введении в питательную среду в количестве от 0,1 до 0,2%. Некоторые грибы, например
растущий на среде с целлобиозой Merulius (Serpula) lacrymans, предпочитают органические фосфаты неорганическому ортофосфату. Содержание фосфора в грибах меняется в зависимости от возраста: в спорах и в молодом мицелии его всегда больше, чем в старом. Например, у Aspergillus niger на третий день культивирования его содержится 12,7 мкг на 1 мг массы сухого мицелия, а на девятый день — 2,4 мкг/мг (Lilly, 1965).
Близкие к этим данным были получены нами (Беккер, Дмитриева и др., 1972) для культивируемого на среде с кукурузным экстрактом и глюкозой A. fumigatus, где общее количество определявшихся фосфорных соединений достигало 22—25 мкг/мг сухой массы мицелия (или 2,2—2,5%). При этом порядка 20—25% от их количества составляли кислоторастворимые полифосфаты, 4—5%—свободные нуклеотиды и около 70%—РНК. Количество ДНК не превышало 7—9% от общего количества определяемых фосфорных соединений, а соотношение между РНК и ДНК составляло почти целый порядок (РНК было в 7—8 раз больше, чем ДНК (табл. 2.4).
|
Таблица 2.4 Количество фосфорных соединений в мицелии Aspergillus fumigatus из трехдневной культуры на качалке на среде с кукурузным экстрактом и глюкозой (по Беккер, Дмитриевой и др., 1972)
|
Для дрожжей указываются еще большие отличия в их концентрациях, а именно отношение ДНК: РНК составляло 1: 50, а общая концентрация нуклеиновых кислот в ядре не превышала 10% от общего количества в мицелии. Такое высокое преобладание РНК над ДНК в клетке является, видимо, характерным для вегетативных форм роста очень многих грибов и отличает их от других организмов.
Калий требуется грибам в количествах, соизмеримых с фосфором (от 40 до 150 мг на литр среды), поэтому в питательных средах они дозируются вместе в виде фосфата калия. Калий весьма специфичен и заменяется натрием и бериллием только частично. Он активирует ряд ферментов (табл. 2.5).
Из объективных данных можно заключить, что при недостатке калия у Aspergillus niger образуется много щавелевой кислоты, т. е. происходит неполное окисление и выделяется NH3 вследствие торможения синтеза или аминирования органических кислот и отсюда торможения синтеза белка. При достаточном количестве калия и недостатке витамина В] происходит торможение декарбок-
|
Таблица 2.5 Извлекаемые нз грибов ферменты, активируемые иоиом калия (Диксои, Уэбб, 1982)
|
силирования продуктов углеводного обмена и накапливается пировиноградная кислота, следовательно, калий участвует в синтезе кетокислот (Lilly, 1965). Механизм действия калия на обмен углерода стал выясняться при изучении его роли в проницаемости и усвоении минеральных компонентов среды и в поддержке в клетке изменяющегося при дыхании и брожении нормального баланса ионов, особенно концентрации Н+.
Оказалось, что К+, Na+ и Н+ имеют одинаковый переносчик через мембрану, но сродство этого переносчика к натрию в 20— 25 раз ниже, чем к калию, что и объясняет незаменимость калия в обмене. В отсутствие К+ (компенсатора) концентрация Н+-ионов в клетке должна повышаться до непереносимого белками плазмы предела вследствие накопления кислых продуктов дыхания и брожения и всасывания анионов, прежде всего Н2Р04~. Отсюда компенсация понижения pH при недостатке калия осуществляется в форме выделения NH3.
Сбалансированное усвоение организмами калия н фосфора объясняется тем, что фосфорная кислота в клетке ведет себя как обменная система анионов Н2Р04_ и ОН-. При усвоении ее среда подщелачивается, а клеточное содержимое подкисляется. Однако К~ способен входить в клетку наравне с Н+ и в 5 раз быстрее других катионов, но обратное вытекание его из клетки в 30 раз меньше, чем Н+ (из клетки способно выделяться 20 мкмоль/кг/ч к+ против 600 мкмоль/кг/ч для Н+). Поэтому концентрация калия в клетке (при pH 6,0) может достигать 200 мкмоль/кг, а Н+ только 0,001 мкмоль/кг и вытекание Н+ из клетки при этом не прекращается.
Таким образом, К+ всасывается из среды избирательно, даже когда внутренняя концентрация его в 5000 раз больше наружной. Натрий всасывается в 20 раз слабее калия, а выделяется намного быстрее.
Следовательно, калий непосредственно не участвует (Rothstein, 1965) в реакциях метаболизма, как микроэлементы и сера, в их энергетическом снабжении, как фосфор, или в композиции клеточных структур, как азот, кислород, водород и углерод. Его функция состоит в конструировании механизма обмена с внешней средой и в поддержании нормальных для обмена физико-химических условий гН, pH, баланса ионов в клетке.
Магний очень необходимый элемент. Потребность в нем близка к потребности в сере, что является обоснованием для применения его в средах в виде MgS04. Aspergillus niger требуется для оптимального роста 20 мг/л Mg2+, Allomyces arbuscula — 9 мг/л.
Содержание магния в мицелии зависит от возраста культуры и типа источника азота. Так, клетки трехдневной культуры мицелия A. niger на среде с аммонийным азотом содержали 0,13%, а с нитратным — 0,26% магния (Lilly, 1965). Можно искусственно обогатить мицелий магнием на богатой им среде.
В дрожжах концентрация магния достигает 292 мкг/кг сырых клеток, но они плохо растут без достаточного количества калия в среде. Эти соотношения объясняются значением калия для усвоения Н2Р04~ и ролью магния в фосфорилировании. Магний является составной частью (кофактором) фосфатаз. Внешне это проявляется в согласованном усвоении обоих элементов: на каждые 36 атомов фосфора требуется 1 атом магния.
Магний играет большую роль в углеводном обмене и всех синтезах на основе использования энергии фосфорных связей. Около 50 ферментативных реакций у грнбов идут с участием магння. Так, 18 фосфокиназ осуществляют фосфорилирование и перенос энергии фосфорных связей с одного соединения на другое, 16 транс — фераз осуществляют с помощью энергии фосфорных связей синтезы с переносом углеродсодержащих фрагментов с одного соединения на другое. Ряд фосфатаз производят отщепление Н2Р04_, ряд синтетаз осуществляют конденсацию с участием фосфорилирова — ния. Другие ферменты также действуют при участии магния (му — тазы, изомеразы, лиазы и редуктазы) (Диксон, Уэбб, 1982).
В синтетазах магний участвует преимущественно совместно с калием. По-видимому, все же не все фосфатазы связаны именно с магнием, так как, например, он активирует у Pйnicillium chryso — genum ферменты, деполимеризующие мета-, пирофосфаты, АТФ при pH 6 и подавляет их при pH 3,5. С другой стороны, он возвращает активность фосфатазам, инактивированным цианидом (Sadasivan,. 1965).
На пектиновые энзимы он влияет также различно в зависимости от оптимума их pH, подавляя энзимы Botrytis cinerea с оптимальным pH 4—5 и активируя энзимы Pythium debarianum с оптимальным pH 8—9 (Ashour, 1954). Магний способен нейтрализовать действие ряда ядов (сулемы, борной кислоты) возможно вследствие антагонизма ионов. Магний сильно угнетает одни биосинтезы биологически активных веществ (например, токсинов уров — ской болезни у Fusarium sporotrichiella var. роае — представляющих собой стероиды или трихотецины) и стимулирует другие (например, образование янтинеллина у P. janthinellum (Беккер, 1963).
Кальций в золе грибов содержится от нескольких единиц до 50%. Особенно часто он встречается в виде щавелевокислого кальция, например в мицелии Merulius (Serpula) Iacrymans. Нередко кальций играет роль нейтрализатора избытка органических кислот, образующихся в обмене многих грибов. В отсутствие его урожай мицелия Aspergillus niger и Fusarium снижается. У некоторых водных форм грибов, например у Allomyces arbuscula, он принадлежит к числу обязательных элементов (Lilly, 1965) и участвует в транспорте аминокислот. Ион Са2+ является также необходимым элементом для роста оомицета Phytophthora infestans, оптимально эффективным в концентрации от 50 до 500 мкМ (Окороков и др.,
1976) (рис. 2.1). Специфичным переносчиком Са2+ в мицелии и
|
lg[Ca2+] Время инкубации, мин і———- 1 і————— 1—- 1 10 )00 500 то 9000 [Са2+], мкМ Рис. 2.1 Рис. 2.2 |
Рис 2.1. Влияние концентрации кальция иа рост Phytophthora infestans. 1—масса сухого мицелия; 2 — накопление в нем Са,+ (Сысуев. 1979)
Рис. 2.2 Влияшк Mg2"1 — АТФ (10 мкМ). Mg2“ РРП (Н> мкМ) и Mgs-t (ПФі (1 мкМ* иа поглощение “Са (1 мкМі проростками Phvtuphthora infestans-, К — контроль (Cucveii I РТР’.
донором энергии оказалась магниевая соль пирофосфата (РРн), тогда как магниевые соли АТФ и полифосфатов (ПФЛ) ингибировали этот процесс (рис. 2.2; Сысуев, 1979). Неорганический фосфат не проявлял действия (Okorokov et al., 1978). Участвующая в освобождении энергии для переноса Са2+ в клетку пирофосфа — таза теряла активность при избыточном введении ионов Са2+ в среду при инкубации in vitro (выше 5 мкМ), что должно вести к прекращению транспорта этого элемента в клетку (Сысуев и др., 1977; Сысуев, 1979). Оптимальная доза Са2+ для роста Phytophthora infestans находится в пределах от 50 до 500 мкМ на грамм сухого мицелия, что составляет порядка от 0,2 до 2 мг на 1 литр культуральной среды. Роль иона кальция для метаболизма Р. infestans в этих работах осталась не вполне ясной. Наблюдаемой в присутствии Са у другого оомицета Achlya стимуляции транспорта аминокислот установить не удалось у Phytophthora (Сысуев и др., 1977). Возможно, что Са замешан в функции проницаемости клеточных мембран этого гриба.
Кальций является составной частью (коферментом) ряда гид- ролаз (табл. 2.6), например а-амилазы и некоторых гидролаз цик-
|
Т абл ица 2.6 Извлекаемые из грибов гидролитические ферменты, содержащие Са2+ (Диксон, Уэбб, 1982)
|
лических полисахаридов (Диксон, Уэбб, 1982). Вероятно, в силу конкуренции с магнием кальций может подавлять активность некоторых фосфатаз у Pйnicillium chrysogenum (Sadasivan, 1965).
Микроэлементы (или следовые элементы) необходимы для обмена в незначительных количествах (тысячных и десятитысячных долях процента, по Стайнбергу, от 0,3 до 0,02 мг/л). К ним относятся железо, цинк, медь, марганец, молибден, кобальт, бор и некоторые другие (для грибов также галлий, скандий). Они входят в состав ферментов. Для изучения потребности в микроэлементах у грибов большую роль сыграли работы Стайнберга (1919), исследовавшего ее на модели Aspergillus niger.
Железо — микроэлемент, требующийся в наибольшем количестве (0,001%), его даже добавляют в среды на водопроводной воде, например в среду Чапека. На среде без железа урожай A. niger снижается в 70 раз. Усваивается железо в основном в форме растворимых неорганических солей (сульфатов и хлоридов), но некоторые грибы удовлетворяются хелатами железа органического происхождения (гемы, цитохромы и другие), например Pilobolus (Page, 1962, цит. по Lilly, 1965). Железо входит в состав ряда важных окислительных ферментов со структурой порфиринов, особенно участвующих в дыхательной цепи и цикле Кребса (табл. 2.7).
Таблица 2.7
|
Извлекаемые из грибов оксигеиазы, гидратазы и дегидрогеназы, активируемые Fe2+ (Диксон, Уэбб, 1982)
|
К числу ферментов, содержащих железб как кофактор, относят каталазу, пероксилазу, цитохромы b и с, цитохромоксидазу и цито — хромпероксидазу, но, кроме того, оно активирует ряд других ферментов. Механизм участия железа в окислительных реакциях представляют обычно следующим образом: Fe2+—л«=fcFe3++к. Сброс электрона с двухвалентного железа сопровождается выделением энергии. Специфическое влияние железа на обмен A. niger состоит в усилении процессов окисления: при дефиците железа образуется больше лимонной кислоты и меньше щавелевой, т. е. в присутствии его достигается более высокая степень окисления. Ввиду того что железо играет роль в некоторых этапах восстановления нитратов, в присутствии его в достаточных количествах некоторые грибы усваивают помимо обычного для них иона NH4+ еще и ион N03~.
Кроме того, ионы железа обладают способностью резко усиливать активность некоторых антибиотиков, например ликомаразми — на у Fusarium oxysporum f. lycopersici. Однако все случаи участия железа в обмене не полностью обосновывают высокую потребность в нем. Более детальный анализ показал, что в окислительных ферментах участвует не более 20% требующегося для нормального обмена количества железа.
До 80% железа оказалось содержащимся в клетках в форме неорганических комплексов с фосфорной кислотой (Кулаев, 1975). Эти соединения, видимо, представляют собой механизм депонирования и детоксикации отщепляющегося при синтезах ортофосфата.
Этот механизм может быть основой для объяснения сходства симптомов хлороза (недостаток железа) и паразитарных токсикозов растений (тоже хлороз), при которых наблюдается как разобщение окислительного фосфорилирования (сброс Н3РО4 без обратного включения в АТФ), так и хелирование железа токсинами паразитов (тогда хлороз является результатом накопления не связанной с железом фосфорной кислоты).
Физиологическое действие металлов часто резко возрастает при их сочетании. Эффект действия на грибы железа сильно возрастает в присутствии цинка. В опытах Стейнберга масса сухого мицелия Aspergillus niger без железа и цинка была равна 18 мг, в присутствии одного железа — 44, одного цинка — 40, в присутствии железа и цинка — 731 мг вместо 44+40=84 мг, если бы эффекты этих микроэлементов просто складывались. Это можно связать с последовательным участием обоих элементов в ферментах дыхательной цепи (в первых ступенях ее — цинк, в последующих — железо).
Оба этих элемента участвуют также в активизации пектиновых энзимов у возбудителя вилта хлопчатника Fusarium oxysporum f. vasinfectum, для которого оптимальная концентрация железа составляет 20—40 мг/кг почвы (при тех же концентрациях магния), а оптимальная дозировка цинка 20 мг/кг почвы (Sadasivan, 1965).
Цинк необходим для очень многих обменных процессов. Потребность в нем доказана для ряда видов Aspergillus, дрожжей, мукоровых грибов, например Rhizopus nigricans, и других зиго — и оомицетов, для ряда сумчатых грибов, патогенных грибов, возбудителей дерматомикозов и т. д. Основная роль цинка как кофактора дегидрогеназ, участвующих в углеводном обмене (табл. 2.8), демонстрируется его влиянием на экономический коэффициент (на увеличение массы сухого мицелия, отнесенного к весу использованных углеводов) и на увеличение выделения С02 (на повышение энергии дыхания).
При недостатке цинка окисление субстрата идет не полностью и в среде получается много побочных продуктов обмена, например органических кислот. В присутствии цинка их образование подавляется. Если источником углерода являются органические кислоты— винная, янтарная, глюконовая и т. д., то влияние дефицита цинка проявляется много слабее, что объясняется его участием в цикле дикарбоновых кислот Кребса. Цинк участвует в образовании, вовлечении в дальнейший обмен и превращении в аминокислоты многих окси — и кетокислот.
Образование фумаровой и молочной кислот у Rhizopus снижается при повышении концентрации цинка, что объясняется его участием как кофермента в дегидрогеназах молочной кислоты, D-2-оксикислот, а также алкоголя, глицеральдегида и т. д. (см. табл. 2.8). Специфичная необходимость цинка для обмена была показана при попытке замены его химически близким кадмием, который мог пополнить дефицит его только при наличии в среде не менее 25 мкг/л исходного количества цинка, и оптимальное ко-
|
Извлекаемые из грибов дегидрогеназы, содержащие Zn2+ (Диксон, Уэбб, 1982)
|
личество кадмия на этом фоне (450 мкг/л) почти вдвое превышало оптимальное количество цинка (250 мкг/л), требуемое в этих условиях (Bertrand, de Wolf, 1961).
Специфический эффект цинка в отношении синтеза у Aspergillus niger аминокислот оказался наиболее выраженным для ароматических аминокислот с бензольным ядром: в первую очередь фенилаланина, а затем триптофана и тирозина, причем замена цинка в этом синтезе кадмием была возможна только для триптофана и тирозина.
Подавление триптофансинтетазы при цинковом голодании было показано для Neurospora. При недостатке цинка у A. niger подавляется (хотя возможно вторично, в результате угнетения обмена углеводов) и синтез алифатических аминокислот—аланина, глицина, пролина, треонина, серина, валина, лейцина, изолейцина, аспарагиновой и глутаминовой кислот.
Влияние цинка на углеводный обмен A niger сказывается и на синтезе нуклеиновых кислот, в котором в первую очередь, вероят
но, страдает биосинтез рибозы и дезоксирибозы. Для них замена цинка через кадмий имеет слабый эффект (Bertrand, de Wolf, 1961). Какие именно из шести известных цинкозависимых энзимов гликолитического и пентозного циклов играют здесь основную роль, сказать трудно. Это могут быть как зависящие от цинка в процессе их синтеза глюкозоизомераза, фосфофруктокиназа и глицеральде — гидфосфатдегидрогеназа, так и содержащие цинк в качестве ко- энзима глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидро — геназа и особенно сильно зависящая от цинка альдолаза.
Участие цинка в образовании многих энзимов объясняется его особой ролью в синтезе их коферментов (ароматические аминокислоты, аминокислоты, НАД и т. д.), что отражается на продуцировании биологически активных веществ и других веществ специального экологического назначения, образующихся в боковых путях обмена. Например, цинк, введенный в концентрациях, в 1000 раз превышающих концентрацию, оптимальную для роста (для роста достаточно 0,001 мг%), резко усиливает образование цитохрома и цитохромоксидазы у Usоilago sphaerogena.
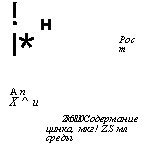
Цинк сильно влияет на образование некоторых токсинов, например токсина уровской болезни (поина) у Fusarium sporotrichi — ella var. poae и других соединений стероидной структуры (Беккер, 1963). Он влияет на образование фузариевой кислоты у F. oxyspo — rum f. vasinfectum (возбудитель фузариозного вилта хлопчатника), стимулируя его в концентрации около 250 мкг/л и угнетая при 400 мкг/л (рис. 2.3) (Kalyanasundaram, Saraswathi — Devi, 1955).
Действие цинка на формирование способности возбудителя вилта образовывать фузариевую кислоту в онтогенезе культуры про-
|
Ч & N. & $ £ * gl »l|l if’ ‘*°s l! iw, о I |
|
М 100 s »! |
|
£0- |
|
100 Ъ’ЪЦЧКонтропьОЛ 0,2 0,3 0,4 0,5 Ofi 0,7 5 s 11 без цинка Концентрация цинка, *= мг/л или мг/кг почвы |
|
! н I* А п X ^ и |
|
Рост |
|
2 k 6 8 10 Содермание цинка, мкг! ZS мл среды |
 |
|||
 |
|||
|
|
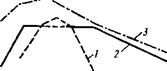

Рис 2 3. Действие цинка на рост и антибиотическую активность Fusarium oxys-
porum f. vasinfectum
Рис 2.4. Зависимость образования фузариевой кислоты в лабораторной культуре от концентрации цинка в среде (/), активность штаммов возбудителя вилта, выделенных из почвы с различным содержанием циика (2), и интенсивное«: заболевания хлопчатника вилтом (3) на тех же почвах (Беккер Полетаева
1971)
является и как селекционирующий фактор. В почве при разной концентрации цинка формируются популяции охузрогит, воспроизводящие уровни активности фузариевой кислоты, свойственные исходной культуре при разных концентрациях цинка в питательной среде (рис. 2.4) (Беккер, Полетаева, 1968). Уровень вил — тового токсина в хлопчатнике также воспроизводит эту кривую токсичности популяции возбудителя. Сопоставление данных спект — рофотометрии пиридинов и активности фузариевой кислоты этих популяций показывает, что увеличение концентрации цинка в почве выше оптимума для синтеза фузариевой кислоты снижает только
|
D, k О,7 2,0 5,0 10,0 Концентрация цинка, мг/кг почбы |
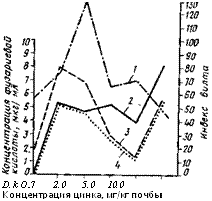 ее синтез, но продолжает увеличивать способность к образованию* нетоксичных соединений этого ряда (Беккер, Полетаева, 1971) (рис. 2.5). Цинк способствует также образованию многих пигмен-
ее синтез, но продолжает увеличивать способность к образованию* нетоксичных соединений этого ряда (Беккер, Полетаева, 1971) (рис. 2.5). Цинк способствует также образованию многих пигмен-
Рис. 2.5. Изменение способности популяций Fusarium oxysporum f. vasinfec — tum к образованию фузариевой кислоты (4) и других пиридинов, определяемых спектрофотометрическим (2) и биологическим (3) методами, и присущая им интенсивность заболевания (/) при их формировании в почве с различными дозами цинка (Беккер, Полетаева, 1971)
тов, например меланина у Macrosporium и хризогенина у Pйnicillium chrysogenum.
Медь имеет более ограниченное значение, чем железо и цинк„ однако и она принадлежит к числу необходимых для грибов микроэлементов. Она требуется Aspergillus niger в количестве порядка
0, 4 мг/л. Однако у Nectria galligena рост продолжает усиливаться и при концентрациях в 10 раз выше. Сильное влияние меди на рост N. galligena объясняется большой ролью ее в обмене тирози — назы (полифенолоксидазы, окисляющей тирозин), присутствующей у многих грибов, особенно у микоризообразующих базидиомицетов. Возможно, что медьсодержащие энзимы этого типа играют у ряда грибов роль в их энергоснабжении.
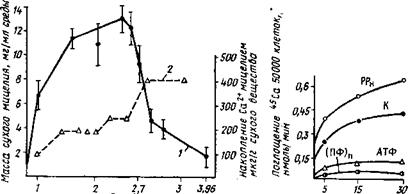
Кроме тирозиназы медь входит в состав таких оксидаз, как лакказа (полифенолоксидаза), оксидаза аскорбиновой кислоты, оксидаза цитохрома а3, уратоксидаза (табл. 2.9), и участвует в этапах восстановления нитратов на ступенях нитрит — и гипонитрит- редуктаз (Lilly, 1965). У A. niger она играет роль при образовании и использовании лимонной кислоты (рис. 2.6). При добавлении в среду цитрата его потребность в меди заметно падает.
Как железо и марганец, медь сильно влияет у грибов на спорообразование и пигментацию спор. По этому признаку с помощью A. niger можно обнаружить концентрации меди в среде порядка
|
Извлекаемые из грибов оксидазы, содержащие медь (Диксон, Уэбб, 1982)
|
0, 05 мкг/50 мл. Медьсодержащие оксидазы, видимо, участвуют также в образовании меланиновых пигментов грибов (табл. 2.9).
Потребность в меди была доказана для A. niger, A. flavus, Rhizopus sp., Sclerotium rolfsii, Cercospora nicotianae, Fusarium oxysporum, Pythium inegulare, Thielavia basicola (Steinberg, 1950). Не исключается, что медьсодержащие оксидазы участвуют также в детоксикации ароматических антисептиков для древесины типа креозота, начиная, таким образом, сукцессию грибов на обработанной ими древесине. Первыми поражают ее грибы, содержащие меланины.
Марганец нужен грибам в очень небольшом количестве порядка 1 : Ю9. Однако он играет существенную роль в обмене как кофактор щавелевоуксусной и щавелевоянтарной карбоксилазы — фермента, участвующего в основной реакции усвоения С02 у ге — теротрофов путем присоединения ее к энолпировиноградной кислоте. Общее число обнаруженных у грибов ферментов, где марганец является кофактором (табл. 2.10), невелико, и они главным образом участвуют в трансформации органических кислот цикла Кребса.
Марганец вместе с медью участвует как кофактор в образовании и потреблении лимонной кислоты у Aspergillus niger и предположительно — в ее синтезе как кофермент аконитазы. Некоторую роль играет марганец и в азотном обмене, активируя аргиназу дрожжей и входя в состав гидроксиламинредуктазы у плесневых грибов (Диксон, Уэбб, 1982). Последний энзим был обнаружен у Neurospora crassa при восстановлении этим организмом гидрок — силамина в аммиак (Lilly, 1965).
Марганец специфично угнетает образование пектолитических энзимов у Fusarium oxysporum f. vasinfectum, конкурируя при этом с железом. При соотношении железа и марганца 1:2 образование пектиновых энзимов у этого паразита хлопчатника падает и соответственно снижается вызываемое им заболевание хлопчатника фузариозным вилтом (Sadasivan, 1965).
|
SAM
-Рис. 2.6. Влияние меди на изменение массы мицелия (1) и содержание лимонной кислоты (2) в культуре Aspergillus niger. Увеличение количества меди в среде выше 6—7 мкг/л приводит к снижению количества лимонной кислоты в культуральной жидкости (Bertrand, de Wolf, 1960) |
Рис. 2.7. Интенсивность заболевания хлопчатника фузариозным вилтом (и. в.— 1) и накопление в нем переносчика метильных групп S-аденозилметионина {SAM — 2) при различных дозировках кобальта в почве (Беккер, Полетаева,
1971)
Молибден требуется грибам в наименьшем количестве по сравнению с другими микроэлементами; обнаружено до сих пор его участие всего в одном метаболическом процессе — восстановлении нитрата в нитрит (первый этап пути восстановления соединений азота осуществляется системой нитратредуктаз). Вероятно, с этим процессом связано участие молибдена в фиксации атмосферного азота у бактерий и сине-зеленых водорослей, в котором играет основную роль система ферментов, названная нитрогеназой (Кре — тович, 1972). Этим объясняется также, что Aspergillus niger на среде с солями NO3- требует больше молибдена, чем на среде с NH4+. Молибден является коэнзимом нитратредуктазы, что подтверждается реактивирующим эффектом добавки молибдена к нит ратредуктазе A niger, инактивированной цианидом
|
Извлекаемые из плесневых грибов дегидрогеназы, редуктазы, дегидратазы и лиазы, содержащие Мп2+ (по Диксону, Уэббу, 1982)
|
В других этапах пути восстановления ЫОз~ кроме молибдена участвуют медь, железо, марганец:
Мо Си, Ре Си, Ре Мп
|
возможно Со
Гидроксил — Амми-
амин ак
Дефицит молибдена у грибов наблюдается редко, однако он возможен в условиях избытка конкурирующей с этим элементом меди. Наоборот, дефицит меди в результате присутствия избытка молибдена в почве мы наблюдали в Ферганской долине, что отразилось на торможении образования антибиотиков типа геодина у почвенных грибов, антагонистов возбудителя вилта.
Хлор необходим грибам в основном для синтеза хлорсодержащих антибиотиков: геодина (A. terreus), гризеофульвина (Pйnicillium nigricans, P. urticae и P. janthinellum), хлорсодержащего метаболита калдариомицина (Caldariomyces fumago), нидулина (A. nidulans), налгиолаксина (P. nalgiovensis) (Miller, 1961). Однако y грибов известен один фермент, в составе коферментов которого имеется хлор (табл. 2.11), это арилсульфатаза-эстераза, расщепляющая ароматические эфиры серной кислоты (Диксон, Уэбб, 1982).
Кобальт принадлежит к числу микроэлементов, обязательных для животных и бактерий, участвуя в составе витамина Bi2 в синтезе метионина и тимидиновой части нуклеотидов ДНК. Выясняется также, что, видимо, он участвует в последнем этапе системы нитратредуктазы (или нитрогеназы), способствуя восстановлению гидроксиламина в аммиак (Ягодин, 1970). Однако необходимость кобальта для грибов пока подтверждена слабо, так как очистить от него среду до уровня, выявляющего его дефицит, пока не уда-
|
Извлекаемые из грибов ферменты, активируемые Мо и СГ ‘(Диксон, Уэбб, 1982)
|
лось, вероятно, вследствие очень малых необходимых количеств кобальта для синтеза ДНК ядер, имеющих у грибов очень малые размеры, особенно в вегетативном мицелии.
Тем не менее существование потребности в витамине В12 ■у дрожжей (Kloeckera brevis), на которых можно его тестировать, и данные о способности к его синтезу у Aspergillus niger (Lilly, 1965) подтверждают необходимость его для грибов. Для экологии грибов-паразитов существенно, что кобальт усиливает метилирующие системы, в частности накопление переносчика метальных групп, S-аденозилметионина, приводящие к детоксикации фитотоксинов грибов, например фузариевой кислоты при вилте хлопчатника (Полетаева, 1969; Беккер, Полетаева, 1971; рис. 2.7, табл. 2.12).
По некоторым данным, в определенных условиях у грибов ■встречается потребность еще в нескольких микроэлементах. Например, галлий по данным Стейнберга стимулирует рост A. niger при добавлении его в количестве 0,02 мг/л, 76 других испытанных микроэлементов не заменяли его.
Скандий оказался необходимым для A. niger при росте его на глицерине как источнике углерода, но на средах с сахарами потребность в нем отсутствовала.
По некоторым данным, бор также способствует росту и развитию грибов.
Существуют микроэлементы, которые сами по себе не необходимы, но влияют на усвоение других микроэлементов и могут частично заменить их или изменить направление обмена и нарушить — баланс обменных процессов.
На фоне избытка необходимых микроэлементов они не влияют на рост, развитие и обмен, но при недостаточных дозах влияют очень сильно как в случае естественного недостатка их в природе, так и при дефиците, создаваемом действием многих неметаллических ингибиторов, таких, как СО, мышьяк, группы SH, CN и другие.
Приведем примеры известных микроэлементов — заменителей и конкурентов.
|
хроматографический анализ экстрактов 4,5 и. НС104 из свежих растений хлопчатника, выросших иа вилтовом фоне без добавки в почву кобальта ^контроль) и с добавкой в иее 0,2 и 2,0 мг/кг СоС12. Система растворителей: этанол — вода — уксусная кислота (65 : 34 : 1). Проявление пятен нингидрином (Беккер, Полетаева, 1971)
|